Parcerias
SARS-CoV-2
Antigen Test
O LumiraDx SARS-CoV-2 Ag Test é um ensaio de imunofluorescência microfluídica para a detecção direta e qualitativa do antígeno da proteína do nucleocapsídeo em amostras de swab nasal e nasofaríngeo de indivíduos com suspeita de COVID-19 ou indivíduos assintomáticos. Usado com a LumiraDx Platform, o teste fornece resultados rápidos no local de atendimento.
Benefícios do teste
O uso do teste LumiraDx SARS-CoV-2 Ag Test no Instrument* LumiraDx permitirá que o médico verifique rapidamente se há infecção, inicie o tratamento adequado e inicie as precauções de isolamento, ajudando a prevenir a disseminação da infecção.
- Fácil de implementar no contexto do local de atendimento
- Desempenho clínico
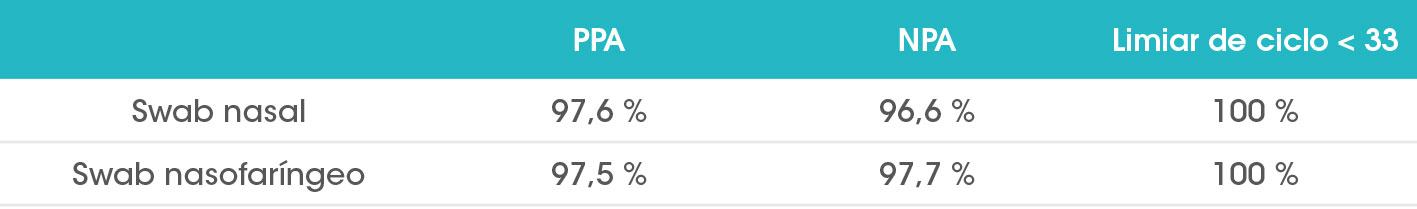
- Concordância percentual positiva de 97,6%
- Concordância percentual negativa de 96,6%
- Desempenho analítico com um limite de detecção de 32 TCID50/mL
- Resultados comparáveis de RT-PCR em até 12 dias após o início dos sintomas
Fluxo de trabalho do teste
O Instrument e os slides de tiras de testes são integrados a várias verificações de controle de qualidade para garantir que o Instrument e o teste estejam funcionando corretamente a cada teste executado.
O processo de fluxo de trabalho é composto por uma preparação de amostra simples, juntamente com a orientação passo a passo do Instrument para relatar o resultado de um paciente em menos de 12 minutos da aplicação da amostra.

Desempenho do teste
Em estudos clínicos, o LumiraDx SARS-CoV-2 Ag Test demonstrou 97,6% de concordância positiva versus RT-PCR em pacientes testados em até 12 dias do início dos sintomas, para permitir que o médico verifique a infecção rapidamente, comece o tratamento adequado e inicie as precauções de isolamento, ajudando a prevenir a propagação da infecção.
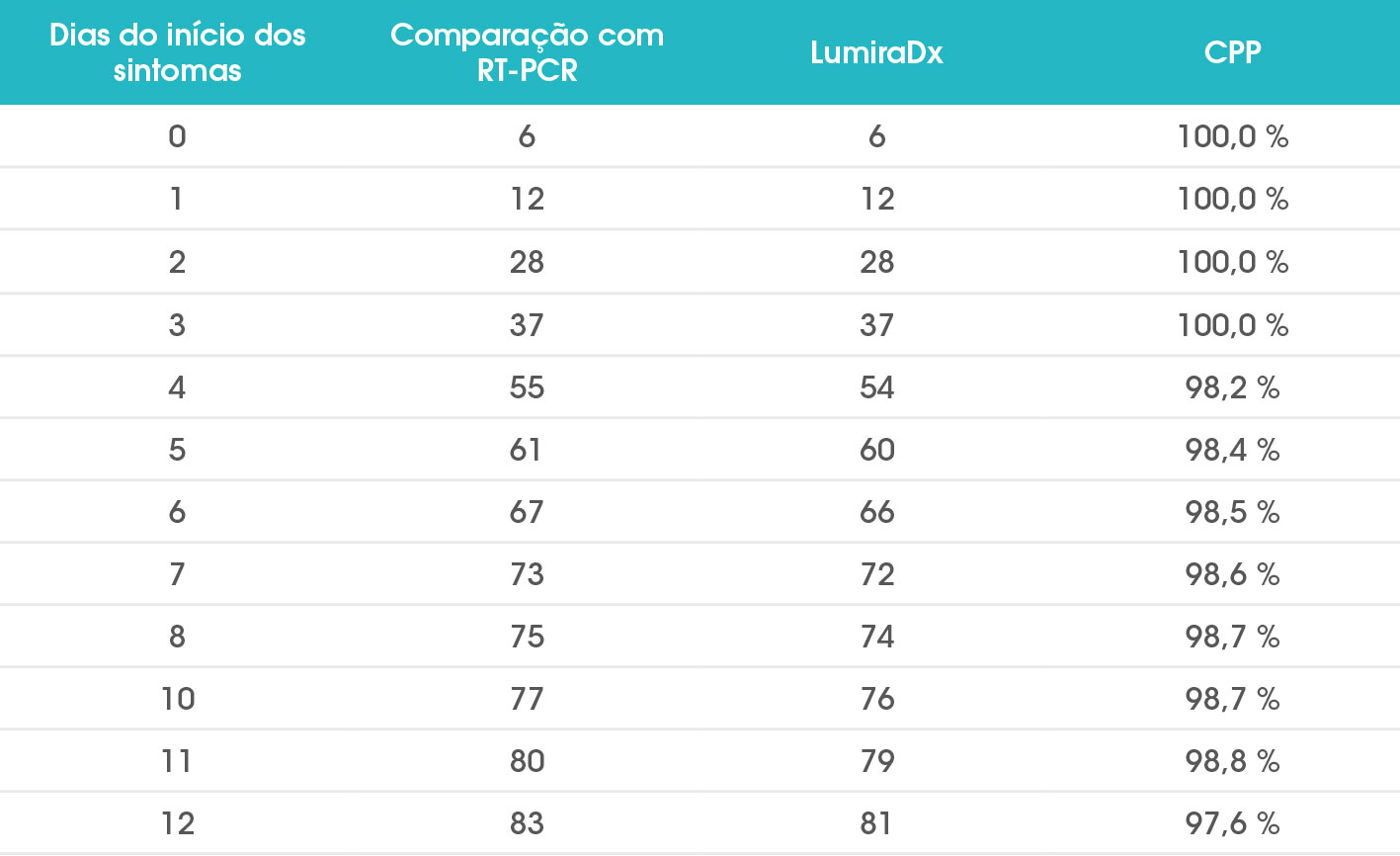
Uma concordância positiva de 100% foi alcançada em amostras com valores de limite de ciclo (ct) <33 (método de referência Roche Cobas 6800 SARS-CoV-2)
Desempenho do método de swab 12 dias após o teste de RT-PCR
Para obter mais informações sobre o
LumiraDx SARS-CoV-2 Ag Test
Nem todos os produtos estão disponíveis em todos os países e regiões. Verifique a disponibilidade em mercados específicos com seu representante de vendas ou distribuidor local da LumiraDx. Disponível nos EUA sob a Autorização de uso emergencial para ensaios para SARS-COV-2.
*Instrument – Nome comercial do instrumento de análise
Melhoresresultadosexperiênciasem saúde
Apoiar vidas mais saudáveis, para a sociedade em geral
Possibilitar relacionamentos responsivos entre os pacientes e profissionais da saúde
Controlar e reduzir custos para ajudar a aliviar a pressão sobre os orçamentos de saúde.