Fast Lab Solutions Informationsportal
Ist es COVID-19?
Ist es Influenza?
Mit Labormethoden vergleichbare Ergebnisse in Minuten
Schneller Nachweis einer potenziellen Infektion mit einem mikrofluidischen POC-Test, der innerhalb von 12 Minuten verwertbare und mit Laborergebnissen vergleichbare Ergebnisse für Patienten mit Verdacht auf Influenza und/oder COVID-19 liefert und so klinische Behandlungsentscheidungen unterstützt.
Vorteile des Tests
- Mikrofluidik-Immunfluoreszenztest
- Für die Verwendung in CLIA-Waiver-Umgebungen zugelassen
- Optimiert Patientenfluss und klinischen Ablauf – 1 Probe, 3 Ergebnisse, 12 Minuten
- Probentyp: Nasalabstrich
- Die vorbereitete Probe kann auch mit dem LumiraDx SARS-CoV-2 & RSV Test verwendet werden*
- Leichte Implementierung am Point-of-Care
- Zeit bis zum Ergebnis: 12 Minuten
- Keine gekühlte Lagerung erforderlich:
Lagerung bei Raumtemperatur (2 °C bis 30 °C) - Tragbares Instrument für die patientennahe Testung
- Minimale Handhabungsschritte
*Der verwendete Abstrichtupfer muss für die Verwendung mit beiden Tests validiert sein - siehe Technical Bulletins Abstrichtupfer
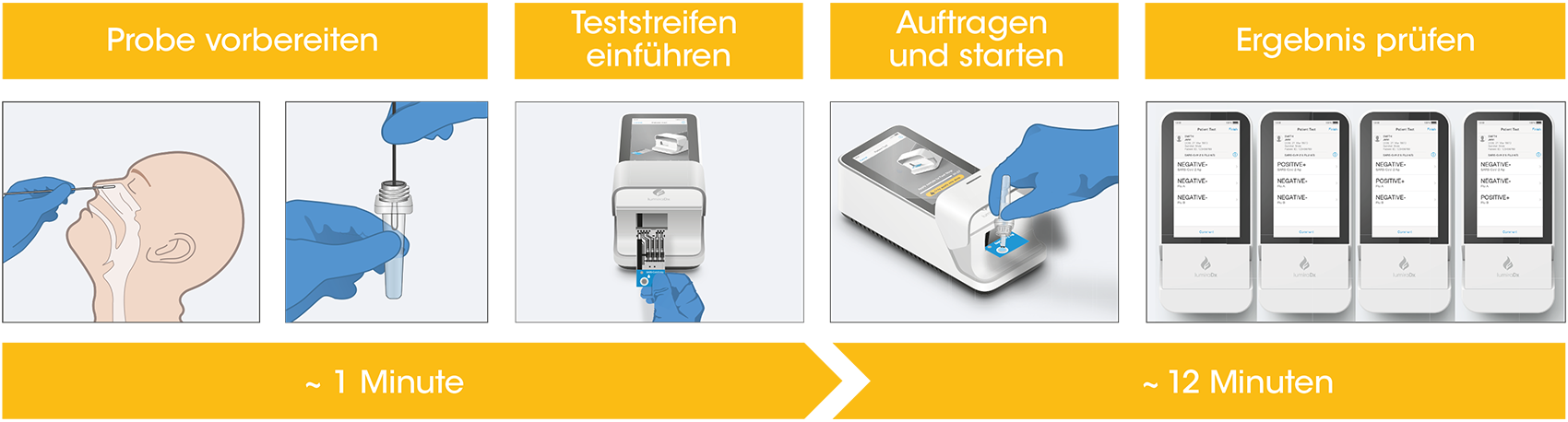
Testablauf
Das Instrument und die Teststreifen verfügen über mehrere integrierte Qualitätskontrollprüfungen, die bei jedem Testdurchlauf die korrekte Funktion von Instrument und Test sicherstellen.
Der Ablauf besteht aus einer einfachen Probenvorbereitung sowie einer schrittweise angeleiteten Testdurchführung durch das Instrument. Das Patientenergebnis wird in weniger als 12 Minuten nach Auftragen der Probe ausgegeben.
Test-Performance
Für den Nachweis von SARS-CoV-2, Influenza A und Influenza B zeigte der LumiraDx SARS-CoV-2 & Flu A/B Test in klinischen Studien eine positive Übereinstimmung von 95,5 %, 83,3 % bzw. 80,0 % gegenüber der RT-PCR.
Klinische Übereinstimmung im Vergleich zur RT-PCR
| SARS-CoV-2 | Influenza A | Influenza B | |
|---|---|---|---|
| PPA | bis zu 95,5 %* | 83,3 % | 80,0 % |
| NPA | bis zu 99,0 %* | 97,6 % | 94,9 % |
*Basierend auf dem Datensatz für 0–12 Tage seit Einsetzen der Symptome. Weitere Einzelheiten siehe Gebrauchsanweisung für den LumiraDx SARS-CoV-2 & Flu A/B Test
Weitere Informationen
zum LumiraDx SARS-CoV-2 & Flu A/B Test:
Nicht alle Produkte sind in allen Ländern und Regionen verfügbar. Bitte erkundigen Sie sich bei Ihrem lokalen LumiraDx-Vertriebsbeauftragten oder -Vertriebspartner nach der Verfügbarkeit in bestimmten Märkten.
KONFORMITÄTSDOKUMENTE
Bessere GesundheitErfahrungenOutcomes
Wir unterstützen ein gesünderes Leben für Einzelpersonen, Communities und die Gesellschaft als Ganzes.
Wir ermöglichen responsive, persönliche Beziehungen zwischen Patienten und Versorgungsteams.
Wir kontrollieren und senken Kosten zur Entlastung des Budgets von medizinischen Einrichtungen.